Exercice n°5 bac Stl BGB Antilles 1995
On donne les potentiels standards des
couples rédox suivants:
couple
1: S2O82- / SO42- E= 2,00 V
couple
2: I2/ I- E=
0,54 V
1. Écrire les équations des couples redox
mis en jeu ainsi que l'équation de réaction susceptible de se produire.
2. Comment peut-on suivre visuellement
l'évolution de la réaction ?
3. Les résultats expérimentaux obtenus
sont les suivants:
|
t(s) |
160 |
450 |
740 |
1080 |
1500 |
1980 |
2400 |
|
[I2] mmol.L-1 |
0.55 |
1.6 |
2.5 |
3.0 |
3.6 |
4.2 |
4.5 |
a)
Définir puis calculer la vitesse moyenne de formation de l'ion iodure I-
sur les intervalles (0 -160 s) et (1500 - 2 400 s).
b)
Définir puis calculer la vitesse instantanée de formation du diiode aux instants t =0 et t =1600 s.
4. En fait cette réaction est lente. Elle
est catalysée par les ions Fe2+.
4.1)
Définir le terme catalyseur.
4.2)
Est-ce une catalyse homogène ou hétérogène ? Justifier.
Corrigé
1.
Couples: S2O82-/SO42-
et I2/I-. D’après
la règle du gamma on a :
S2O82- + 2é = 2 SO42-
et 2I- = I2 + 2é
soit S2O82- + 2I- = 2SO42-
+ I2
2.
On a une
évolution de la couleur de la solution, puisque le diiode est coloré, la
solution devient progressivement orange/marron.
3.
a- courbe : C
est exprimé en mmol.L-1.
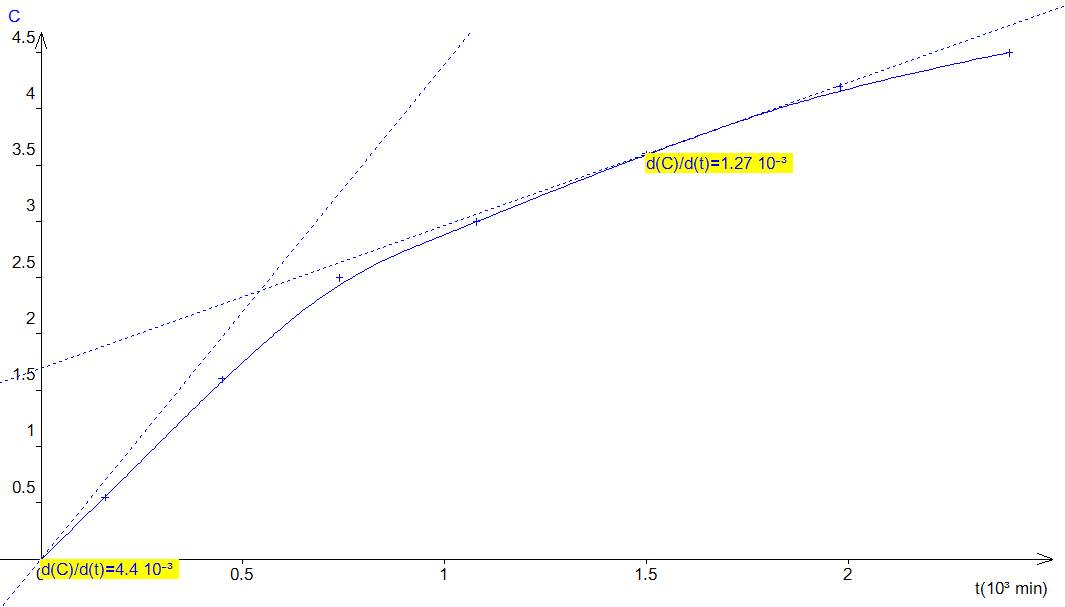
b- vitesses moyennes : Vm0
= (C160 – C0) / (160 – 0) = 3.4 10-6 mol.L-1.s-1.
Vm1= (C2400
– C1500) / (2400 – 1500) = 1.0 10-6 mol.L-1.s-1.
c- Vitesse instantanée de formation d’un produit dont la
concentration est notée C(t). V= dC(t)/dt. On l’obtient en calculant le
coefficient directeur de la tangente au point de la courbe d’abscisse t.
Coefficient directeur de la tangente à l’origine : a= 4.4
10-3 mmol.L-1.s-1 = 4.4 10-6 mol.L-1.s-1.
Donc V= 4.4 10-6 mol.L-1.s-1.
Coefficient directeur de la tangente au point de la courbe
d’abscisse t= 1500s :
a = 1.3 10-6
mol.L-1.s-1 donc V’ = 1.3 10-6 mol.L-1.s-1.
4.
a-
catalyseur : Substance capable d’accélérer une réaction chimique sans
apparaître dans l’équation bilan.
b- Il s’agit d’une catalyse homogène puisque les ions fer II
sont en solution, donc dans une phase liquide comme le reste. Tout est dans le
même état physique.