Exercice n°4
Le nucléide 90227Th
du thorium est radioactif a.
1. Ecrire l’équation nucléaire de cette désintégration.
2. Calculer le nombre de noyaux présents dans une masse m0
= 1.0 mg de thorium. On fera l’approximation
que la masse d’un atome de thorium correspond à la somme des masses de ses
nucléons (avec mp ![]() mn =
1.66 10-27 kg).
mn =
1.66 10-27 kg).
3. A une date prise comme origine t=0, on dispose de l’échantillon
contenant N0 noyaux de thorium radioactifs. A une date t, on
détermine le nombre N de noyaux non désintégrés. On obtient le tableau suivant :
|
t (jours) |
0 |
4 |
6 |
10 |
15 |
20 |
|
N/N0 |
1 |
0.86 |
0.79 |
0.68 |
0.56 |
0.46 |
|
-
Ln (N/N0) |
|
|
|
|
|
|
a- Définir la période radioactive du thorium et en donner
un encadrement à l’aide du tableau ci-dessus.
b- Compléter le tableau et tracer la courbe –ln (N/N0)
= f(t).
c- En déduire la valeur de la constante radioactive l et celle de T.
Corrigé
1. 22790Th → 22388Ra + 42He
+ γ
2. Masse d’un noyau radioactif : m = 227 x 1.66 10-27
= 3.768 10-
Nombre
de noyaux : N0 = m0/m = 1.0 10-9/
3.768.10-25 = 2.65 1015 noyaux. On a négligé les
électrons.
3. a- Définition de la période radioactive :
Durée T au bout de laquelle la moitié d’une quantité donnée de radionucléide s’est
désintégrée.
On voit que T est comprise entre 15 jours et 20 jours
puisque pour t=T on aurait N/N0= 0.5 (Il ne reste que la moitié des
noyaux initiaux…)
b-
|
t en jours |
0 |
4 |
6 |
10 |
15 |
20 |
|
N/N0 |
1 |
0.86 |
0.79 |
0.68 |
0.56 |
0.46 |
|
-Ln (N/N0) |
0 |
0.151 |
0.235 |
0.385 |
0.580 |
0.777 |
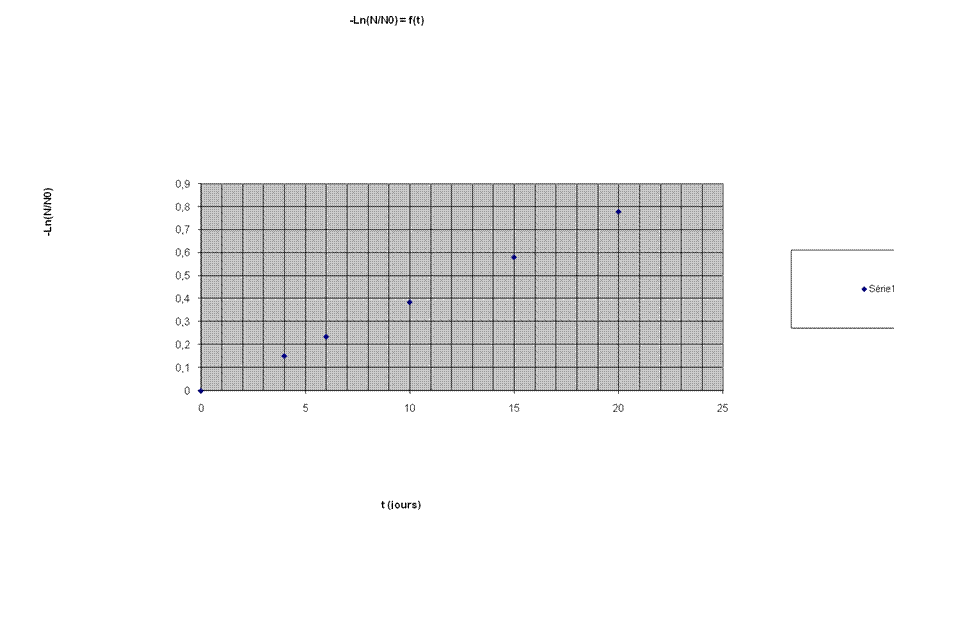
c-
Sur le graphique ci-dessus on peut lire – ln (N/N0) = f(t).
Or
d’après le cours N(t) = N0 e-lt soit N/N0
= e-lt ou encore ln
(N/N0) = -lt soit – ln (N/N0) = λt donc λ est le coefficient
directeur de la droite en jours-1.
λ= yb-ya /(xb-xa)
soit λ= (0.385-0)/(10-0) =0.0385 j-1 environ.
T
= Ln2 / λ = 0.693 / 0.0385 = 18 jours environ. Ce résultat est cohérent
avec la réponse donnée en a.